
Intérêt du dépistage de la vaginose bactérienne
La vaginose bactérienne est l’infection la plus fréquente et concernerait 23 à 29 % des femmes en âge de procréer. Bien que pauci- ou asymptomatique, elle peut être responsable d’une augmentation des infections sexuellement transmissibles, de maladies inflammatoires pelviennes, de prématurité, et peut jouer un rôle dans l’infertilité. Même si le traitement est efficace à court terme, il n’est pas recommandé de réaliser un dépistage et un traitement systématiques de la vaginose bactérienne en population générale asymptomatique, du fait d’un taux de récidive élevé à trois et à six mois et de l’absence de bénéfice retrouvé par les études dans ces populations. Cependant, le dépistage et le traitement systématiques de la vaginose bactérienne peuvent avoir un intérêt chez les femmes enceintes et/ou à risque de prématurité, et dans le bilan initial d’infertilité.

Tests salivaires en pratique, comment en faire bénéficier mes patientes ? Centre expert en endométriose
L’endométriose concerne environ 10 % des femmes en âge de procréer et reste associée à un retard diagnostique moyen de plusieurs années, malgré la diffusion de recommandations nationales dédiées [1]. En France, les recommandations conjointes de la Haute Autorité de santé (HAS) et du Collège national des gynécologues et obstétriciens français (CNGOF) de 2018 rappellent que le diagnostic repose prioritairement sur l’interrogatoire ciblé, l’examen clinique pelvien et l’imagerie (échographie pelvienne de référence, puis IRM en seconde intention), la laparoscopie n’étant plus recommandée comme examen de première intention [2]. Dans ce contexte d’errance diagnostique persistante et de volonté de limiter les cœlioscopies purement diagnostiques, le développement d’un test salivaire fondé sur une signature de micro ARN (Endotest®, Ziwig) représente une avancée majeure [3].

Le risque cardiovasculaire chez la femme : le rôle du score calcique et du scanner coronaire
Les maladies cardiovasculaires tuent plus les femmes que les hommes. Les traditionnels facteurs de risque sont une aide imparfaite à l’identification des femmes les plus à risque. Le score calcique, scanner réalisé sans voie veineuse ni injection d’aucune sorte a révolutionné la prévention car c’est le prédicteur du risque cardiovasculaire le plus puissant dont on dispose actuellement : un score à zéro signifie un risque particulièrement faible, le risque augmente ensuite proportionnellement au score. À partir de ce résultat et de l’ensemble des données cliniques de la patiente, il est possible d’élaborer une stratégie de prévention individualisée.
Le scanner coronaire – réalisé après injection de produit de contraste – est indiqué chez les patientes se plaignant de signes fonctionnels thoraciques et chez lesquelles il existe une suspicion de sténose coronaire significative.

Dépistage HPV : forces, limites et perspectives
Le cancer du col de l’utérus est évitable grâce au dépistage et à la vaccination contre les papillomavirus humains (HPV). Le test HPV, plus sensible que la cytologie pour détecter les lésions précancéreuses (CIN2+), est aujourd’hui recommandé comme méthode de dépistage primaire chez les femmes de plus de 30 ans. Négatif, il permet d’espacer les tests à 3-5 ans. Positif, sa spécificité plus faible génère une augmentation des colposcopies et des interventions inutiles, surtout au premier cycle du dépistage. Les modélisations et les données de vie réelle des programmes de dépistage organisés (Pays-Bas, Canada, Australie, Danemark, Angleterre) confirment ses bénéfices en termes de prévention secondaire, tout en soulignant l’importance de stratégies de triage adaptées.
L’autoprélèvement, efficace et bien accepté, élargit l’accès au dépistage, mais nécessite un encadrement rigoureux pour limiter les faux positifs. Chez les femmes vaccinées, le dépistage reste pertinent, mais doit être espacé et adapté au risque résiduel. L’intelligence artificielle (IA) offre une solution prometteuse pour optimiser la colposcopie et réduire le surdiagnostic, notamment dans les contextes à faible expertise. Des outils comme Cervital montrent une précision supérieure à celle des experts, tout en permettant d’éviter des conisations inutiles.
Pour garantir l’efficacité du dépistage HPV, il est essentiel de mettre en place des algorithmes robustes, de former les professionnels, d’informer les patientes, et de suivre les indicateurs clés. L’IA devrait s’imposer comme un outil d’aide à la décision fiable, complémentaire à l’expertise humaine.

Actualités en gynécologie médicale d’après les communications du congrès de Gynécologie Obstétrique Pratique à Paris, en mars 2025
L’endométriose est maintenant connue pour être une pathologie inflammatoire complexe, multifactorielle et systémique, avec notamment une participation génétique. Elle est associée à d’autres comorbidités telles que le syndrome de l’intestin irritable, les migraines, la fibromyalgie, l’asthme ou les allergies… L’endométriose est également reconnue comme ayant un impact majeur sur la qualité de vie des patientes et est associée également à des symptômes d’asthénie, de dépression, d’anxiété, aux troubles alimentaires et aux dysfonctions sexuelles.
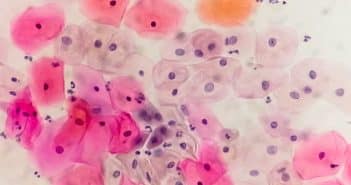
Fiche pratique : Dernières recommandations concernant le dépistage HPV chez les patientes VIH
Les cancers sont une comorbidité fréquente chez les personnes vivant avec le VIH (PVVIH), d’autant que leur espérance de vie augmente, en particulier grâce aux traitements antirétroviraux (ARV) [1].
Les PVVIH doivent bénéficier des programmes de dépistage et de prise en charge pour une affection maligne tels que recommandés en population générale. Cependant, certains cancers ont une incidence plus élevée chez les PVVIH tels que le cancer du col de l’utérus et du canal anal, et doivent bénéficier d’un dépistage spécifique.

La colposcopie chez les femmes immunodéprimées : avez-vous bien tout regardé ?
Patiente de 48 ans adressée en colposcopie après un frottis LSIL (lésions intraépithéliales de bas grade). Elle est suivie pour une polyarthrite rhumatoïde traitée depuis 10 ans par méthotrexate et biothérapie. Non fumeuse, sous microprogestatif, asymptomatique. Dernier frottis normal (janvier 2024).
Vaccination contre le papillomavirus : questions-réponses fréquentes en 2025
Les virus HPV sont ubiquitaires et sont une des plus importantes maladies sexuellement transmises dans le monde. Nous ne devons pas nous arrêter à ce caractère sexuel car ce sont surtout des virus pourvoyeurs de cancers génitaux et oropharyngés.
80 % des adultes en activité sexuelle s’infecteront au cours de leur vie, majoritairement jeunes et souvent dès les premiers rapports. Les cancers surviennent 10 à 30 ans après l’infection. La prévention secondaire basée sur le dépistage est encore nécessaire mais insuffisante. La prévention primaire ne peut être assurée que par la vaccination. Elle est efficace, permettant de prévenir 88 % des cancers du col lorsqu’elle est effectuée avant l’âge de 17 ans. Pratiquée plus tard, elle le reste encore (55-60 %).
Depuis 2007, près de 500 millions de femmes ont été vaccinées dans le monde, sans qu’aucune alerte de tolérance n’ait été confirmée. La vaccination du garçon, débutée dès 2011 aux États-Unis, n’a démarré en France que depuis 2021. Elle est tout aussi indispensable, efficace et bien tolérée. Même chez les femmes déjà infectées, voire déjà porteuses de lésions HPV-dépendantes, la vaccination pourrait avoir un intérêt réel qui nécessite d’être confirmé ou pas.
Le seul problème de ces vaccins, universellement adoptés sous l’impulsion de l’OMS, est celui de la mauvaise couverture vaccinale en France. L’améliorer doit être un combat de tous les professionnels de santé concernés [1].

Éditorial : Le papillomavirus chez les patientes immunodéprimées
Chères lectrices, chers lecteurs,
Dans ce numéro de Réalités en Gynécologie-Obstétrique, nous vous proposons un dossier spécial sur la thématique de l’infection par le papillomavirus, en particulier dans les situations d’immunodépression.
L’infection par le papillomavirus et ses conséquences représentent un enjeu de santé publique, et le gynécologue est un acteur central dans la prise en charge des femmes concernées. Par ailleurs, des recommandations pour le dépistage chez les femmes vivant avec le VIH ont été publiées il y a un peu plus d’1 an. Il nous a ainsi semblé pertinent de faire un état des lieux des connaissances et recommandations sur ce sujet.

Perturbateurs endocriniens et grossesse
Les perturbateurs endocriniens ont littéralement envahi notre quotidien. Capables d’interférer avec les systèmes de régulation hormonale et d’induire des effets délétères sur notre santé, leur impact sanitaire semble d’autant plus préoccupant dans la période clé de vulnérabilité des mille premiers jours de vie.
Si les données sur la santé des futurs enfants sont assez fournies (malformations génitales, anomalies du développement neuro-cognitif, troubles métaboliques et cancers hormono-dépendants à plus long terme), la patiente gestante exposée aux perturbateurs endocriniens est également plus à risque de développer une hypertension gravidique ou un diabète gestationnel, avec un surrisque de prématurité. Il est donc primordial que le clinicien puisse fournir des messages clairs à ses patientes, de manière à limiter au maximum leur exposition et ainsi espérer diminuer les effets néfastes de ces molécules à court et long terme.






